ClonExpress Ultra One Step Cloning Kit
兼容单片段、多片段、入门克隆的一步法克隆试剂盒

快速克隆;高通量克隆;无缝克隆;DNA定点突变;双链DNA与载体组装

· 快速:5 - 15min快速重组
· 简单:一管式Mix,操作简便
· 高效:高效克隆50 bp~10 kb片段,阳性率>95%
· 兼容:单片段、多片段、入门克隆三合一
· 零背景:提供零背景、氨苄/卡那双抗性载体
· 提供在线引物设计:提供在线引物设计软件CE Design
1.高度简化的实验流程
通过PCR扩增,使插入片段5’和3’最末端分别带有和线性化载体两末端一致的序列(15 - 20 bp)。用2 × ClonExpress Mix,50℃反应5-15 min,进行重组。重组产物直接转化感受态细胞,平板上会形成数百个单克隆供阳性筛选。
2.优异的克隆效率
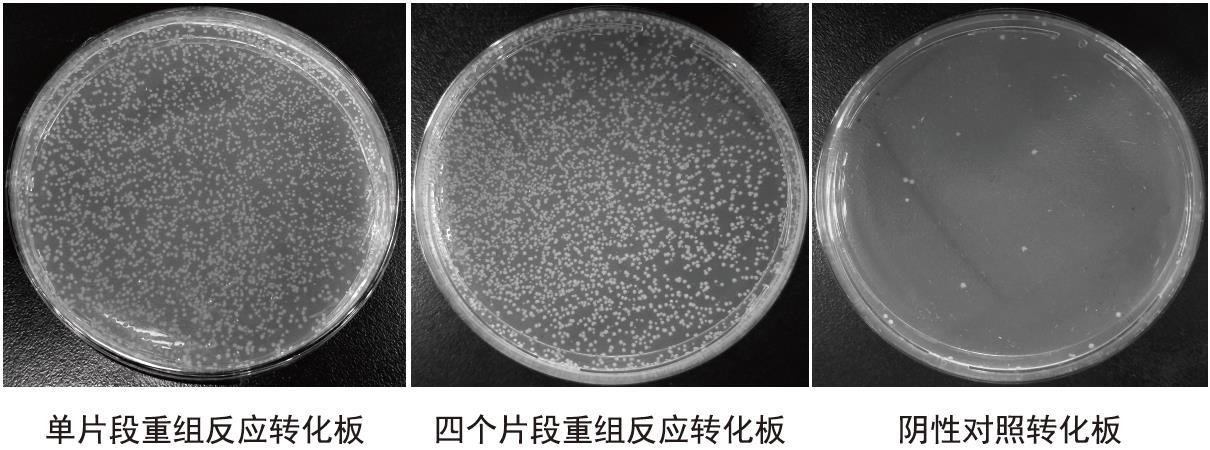
试剂盒能够高效克隆50 bp-10 kb片段,不同长度单片段50 bp、2 kb、4.5 kb、7.5 kb、10 kb;多片段:四个片段(3 kb)、三个片段(10 kb)、五个片段(3 kb)、五个片段(6 kb),纯化后分别与pCE-Zero vector进行同源重组,重组产物转化化学感受态细胞DH5α(Vazyme #C502),菌落数如下图所示。
试剂盒独特的非连接酶依赖体系,无载体自连,克隆阳性率高达95%以上。重组产物转化平板后,各挑取50个单克隆进行菌落PCR鉴定,不同长度插入片段阳性率如下图所示。
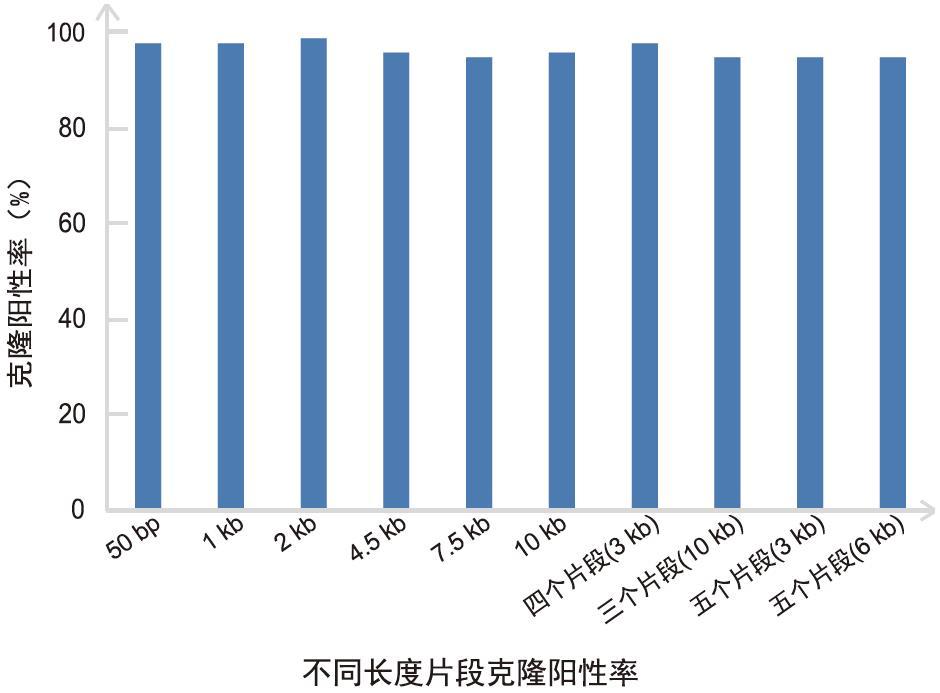
3.广泛的体系兼容性
试剂盒兼容1至5个片段同源重组,搭配Vazyme高保真酶,PCR产物可不经过纯化直接进行克隆。重组产物转化化学感受态细胞DH5α(Vazyme #C502),XL10(Vazyme #C503),Fast-T1(Vazyme #C505),得到较高克隆效率。
4.载体序列信息及测序方案
pCE-Zero vector载体,测序时使用通用测序引物(M13)即可。

本试剂盒作为新一代的重组克隆试剂盒,可快速、高效的将1 - 5个片段定向克隆至任意载体的任意位点。该试剂盒独特的非连接酶依赖体系,降低了载体自连背景,且无需考虑插入片段自身携带的酶切位点。操作简便快捷,50℃条件下仅需5 - 15 min即可完成重组反应。

|
组分 |
C115-01(25 rxns) |
C115-02(50 rxns) |
|
2 × ClonExpress Mix |
125 μl |
2 × 125 μl |
|
pCE-Zero vector,linearized (50 ng/μl) * |
25 μl |
50 μl |
|
500bp control insert (20 ng/μl) |
5 μl |
5 μl |
*双抗性载体:Amp+,Kan+

- 20℃保存。
C115
Q1:引物如何设计?
引物由三部分组成:同源臂(15-20 bp,不计算酶切位点和残留碱基,GC含量40%-60%)+酶切位点(按需保留或舍弃)+特异性引物(引物Tm值由特异性序列决定,计算不包括同源臂和酶切位点的序列)
- 引物设计:官网引物设计软件CE Design,选择相应模块进行设计。
- 载体的线性化方式有三种:双酶切、单酶切和反向PCR,优先选择双酶切;
Q2:阳性对照不长斑或很少。
- 平板抗性使用错误:C112,C113试剂盒中提供的对照载体的抗性为Amp+抗性,C115对照载体的抗性为Amp+,Kan+双抗性;
- 感受态细胞效率低:确保转化效率>107cfu/μg,可进行简单检测,将1 ng质粒转化至100 μl感受态细胞中,取1/10进行涂板,生长1000个菌斑,估算感受态转化效率为107cfu/μg;重组产物的转化体积不应超过感受态细胞体积的1/10,否则会降低转化效率;感受态选择克隆感受态(如DH5α/XL10),不能用表达感受态。
Q3:平板上长不出克隆/克隆数很少/空载体
- 阳性对照:用于排查是否因为操作原因、感受态效价下降、试剂酶活下降导致的重组效率低。
- 引物设计不正确:引物包含15-20 bp同源臂(不计算酶切位点),GC含量40%-60%;若同源臂的长度小于13bp或者大于35bp,基本没有重组活性,长度大于25bp,重组效率会有明显下降;GC含量过高或过低,会影响重组效率。
- 载体线性化方式:尽量选用双酶切,若为快速酶切,建议延长酶切时间(若无星号活性可以过夜酶切),减少质粒的投入量,采用胶回收进行纯化以降低载体未被切开的概率,也可以做阴性对照来验证载体线性化程度。
- 载体和插入片段未切胶回收:未纯化DNA有可能会抑制重组反应, 建议线性化载体、PCR产物进行凝胶回收纯化,纯化产物溶解在ddH2O中。
- 线性化克隆载体和插入片段浓度测定不准确。如果使用NanoDrop测定浓度,必须保证浓度值大于20ng/μl,同时OD260/280在1.8附近,才能保证得到的浓度较为准确,否则需要跑胶鉴定其浓度或重新制备片段(多管浓缩以增加回收浓度)。
- 线性化克隆载体和插入片段扩增产物的使用量不足/过量,即比例不佳:严格按照说明书推荐的量和比例配制重组体系,各组分添加不低于1μl(避免低体积添加造成量取不准)。
- 重组体系:对于C112/C113,重组体系为20μl,10μl重组体系容易造成重组效率低。
- 重组条件:反应需要在精密仪器中进行,如PCR仪、金属浴等,不建议在水浴锅、恒温箱中进行重组,后者可能因为温度不准确造成重组效率下降。
- 感受态细胞的转化效率需大于107cfu/μg,重组产物的转化体积不应超过感受态细胞体积的1/10,否则会降低转化效率;选择克隆用感受态细胞(如DH5α/XL10),不能选择表达用感受态细胞。若为自制的感受态细胞需要测定效价(将1ng质粒转化至100μl感受态细胞中,取1/10进行涂板,生长1000个菌斑,估算感受态转化效率为107cfu/μg),且涂板时需将感受态细胞全部涂在平板上;感受态转化温度准确。
- 增加重组效率的辅助手段:对于C112可以等比例减半载体与片段的投入量。
- 除此之外,需要检查抗生素抗性有未加错。
Q4:假阳性/测序无信号/空载体
- 阴性对照:用于排查是否是质粒载体残留导致的假阳性,如果阴性对照长了很多,可能是模板投入量过多或者未进行DpnI消化。
- 以质粒为模板PCR获得片段/载体:质粒投入量不宜过多(<1ng),否则可能导致DpnI消化不完全从而造成假阳性。建议PCR产物进行凝胶回收纯化,纯化产物溶解在pH 8.0的ddH2O中。
- 挑斑方法:建议选取平板上某一块区域,同时挑选大斑和小斑。主要原因是有以下几点:重组产物3'端与5'端未连接,需要到感受态细胞中进行修复,斑点相对来说会小点;另外板子营养不均匀会导致斑点大小有差异;重组质粒相对原始质粒来说,有可能会影响细胞的生长。所以建议挑取大小斑点,以增加挑到重组产物的概率。
- 菌检引物:建议使用载体通用引物或者引物一端在载体上,一端在目的片段上。如果用目的片段引物进行菌液PCR,可能会出现菌检有结果而测序无结果。
Q5:菌液PCR无条带
⑴ PCR体系或程序不合适:没有目的条带也没有空质粒条带,建议优化PCR体系、程序;或者提取质粒,以质粒做模板PCR验证,或进行酶切验证。
⑵ 重组失败:只有空质粒的条带,说明重组不成功,载体线性化不完全,建议优化酶切体系,检查引物设计。
⑶ PCR试剂不合适:试剂不适合粗品,或者是超出了试剂的使用范围,扩增的片段太大。
Q6:多数克隆含有不正确的插入片段
⑴ PCR产物混有非特异性产物:优化PCR体系,提高特异性;胶回收PCR产物;鉴定更多的克隆。
⑵ 反应体系中混入了相同抗性的质粒:PCR扩增模板为环状质粒时,如扩增产物直接用于重组反应时需进行DpnI消化,或者进行胶回收纯化。
Q7:插入片段出现碱基突变
- 测序的样本数:如果只测了一个样本,不一定可信,需要多测几个样本。
- 分析测序结果:检查突变处的测序信号是否有问题,若为双峰或者杂峰则不一定可信。
- 检查突变位点:如果多个结果突变位点一致,可能是从模板上的引入的或者模板序列与NCBI上不一致。
- 插入片段在PCR获得时使用高保真的聚合酶。
- 若引物处发生碱基突变,考虑是引物合成问题,建议重新合成引物进行实验。
相关产品
FastPure Gel DNA Extraction Mini Kit
DC301-01
2 × Phanta Flash Master Mix(Dye Plus)
P520-01/02/03
C505-02/03
P222-01/02/03/04
DC201-01
GR501-01/02





