HiScript Q RT SuperMix for qPCR (+gDNA wiper)
预混液形式的两步法qPCR专用逆转录试剂(去基因组)

第一链cDNA合成;逆转录(含gDNA去除);基因表达分析;两步法qRT-PCR检测

· 即用型的SuperMix 预混液使用方便省时
· gDNA wiper Mix 可迅速去除基因组污染

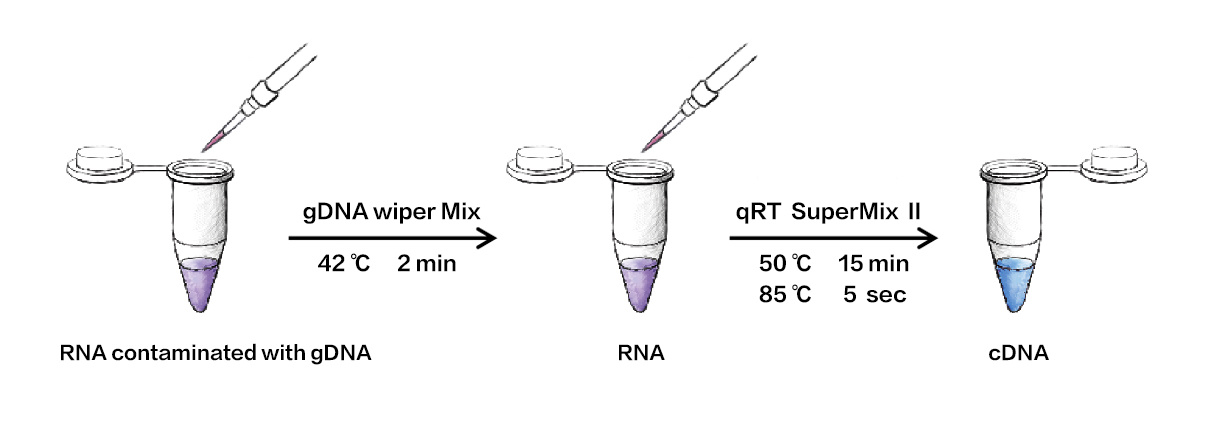
HiScript 两步法RT-qPCR 系列试剂盒(含gDNA 去除模块)以高性价比的HiScript Reverse Transcriptase 为基础,对反应体系进行大幅简化,即用型的SuperMix 将合成高质量第一链cDNA 所需的所有成分合并为一管5 × SuperMix,只需加入RNA和水即可进行逆转录反应,且SuperMix 在-20℃不会冻结,使用方便。产品中包含的4 × gDNA wiper 可在逆转录前快速去除体系中潜在的基因组干扰。本产品操作简便,降低操作过程中的污染机率。合成的cDNA 可以用于SYBR Green qPCR 分析法和探针分析法,进行高性能的基因表达分析。




-30 ~ -15℃保存。
Q1:原核生物RNA能用我们的逆转录试剂吗?
A1:可以。原核生物RNA没有polyA尾,所以在逆转录反应体系中需要以Random primer作为逆转录引物。
Q2:逆转录试剂盒中带有gDNA wiper Mix,可以去除残留在RNA中的基因组。最多可以去除多少的基因组?但如果不进行基因组去除,会影响接下来的逆转录吗?
A2:我们做过100ng基因组的测试,去除效率是99.95%。如果不进行基因组去除不会影响逆转录实验的进行,但是如果基因组残留严重但不去除的话,会影响接下来定量实验的准确性。
Q3:延长逆转录时间,是否可以提高逆转录效率?
A3:对于大多数基因,延长逆转录时间对逆转录效率并没有显著提升;对于一些GC含量较高或含高级结构的模板,延长逆转录时间可提升逆转录效率。
Q4:做了No RT Control发现有gDNA残留怎么办?
A4:如果使用试剂盒中的gDNA wiper模块进行gDNA去除,但No RT Control仍有CT值,可通过实验组和No RT Control组的CT值来判断实验数据是否可用。当实验组CT值与No RT Control对照组CT值差值大于5,说明由gDNA导致的误差小于5%,则可以忽略gDNA污染;若实验组与对照组CT值差值小于3或者几乎一致,则实验组扩增产物的模板很大一部分来源于gDNA,这样的实验组就失去定量意义。
Q5:如何评判RNA质量?
A5:RNA质量从两个方面反应:
(1) RNA完整度。通过琼脂糖凝胶电泳验证RNA完整度。以真核生物为例,完整的总RNA有清晰的三条带,分子量从大到小分别为28S、18S、5S,并且28S是18S亮度的两倍;若能看见三条带,但带型模糊或弥散,则说明RNA有部分降解,此时请立即进行逆转录反应,并适量加大模板量;若只能看见分子量很小的一条带或没有条带,则 RNA 已完全降解,需要重新提取。
(2) RNA的纯度。RNA的纯度可以通过OD260/280和OD260/230两个比值是否在1.8-2.1范围内进行判断,蛋白、离子等残留会使比值降低。
Q6:如何选择逆转录的引物?
A6:根据实验的具体情况选择随机引物、Oligo dT或基因特异性引物进行逆转录。
(1) 随机引物:随机结合在RNA的任何区域,适用于rRNA、mRNA、tRNA等所有RNA类型的逆转录反应。
(2) Oligo dT:适用于具有PolyA尾的RNA(原核生物RNA、真核生物的rRNA和tRNA不具有PolyA尾)。 由于Oligo dT结合在PolyA尾上,所以对 RNA 样品的质量要求较高,即使有少量的降解也会使全长cDNA合成量大大减少。
(3) 基因特异性引物:与模板序列互补,适用于序列已知的基因逆转录。
cDNA后续进行PCR扩增长片段,一般用Oligo dT或者基因特异性引物,不建议使用随机引物,因为随机引物是随机结合的,cDNA片段会偏短,可能会对长片段扩增造成稀释,后续扩增不出全长的目的基因;cDNA后续进行qPCR,一般使用Oligo dT和随机引物的混合物,可以避免3’端和5’端的扩增偏好性。
Q7:可以通过测逆转产物cDNA浓度判定逆转效率吗?
A7:不可以,逆转录产物cDNA是混合物,除了cDNA产物以外,还有buffer、逆转录酶、引物,同时还包含未转录的模板RNA,总RNA中的tRNA、rRNA等,都会干扰浓度测定结果,因此不能反应真实的cDNA产量。
相关产品





