Multiplex PCR Kit

多重PCR扩增;微量样本的多位点检测;高GC体系

· 多重性:检测重数可达19重甚至更高。
· 均一性:扩增稳定均一,靶点偏好性低。
· 适应性:广泛兼容各种GC含量和长度的扩增子,随酶附赠GC Enhancer。
· 特异性:扩增缓冲高度优化,较大程度上抑制非特异性扩增。
· 灵敏性:使用基因组DNA作为模板,扩增灵敏度可达1 ng。
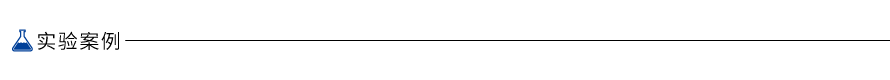

Multiplex PCR Kit具有值得信赖的扩增能力和灵敏度,能在默认条件下高效完成大多数多重扩增反应。如图所示,以人基因组为模板进行19重检测,扩增子长度范围为70 bp-916 bp。可见,在1 ng-500 ng的模板量范围内Multiplex PCR Kit都可以均一的对各位点进行多重扩增。
M: 100 bp DNA Ladder
Multiplex PCR Kit具有优异的片段长度兼容性。如图所示,以小鼠基因组DNA为模板,扩增1.55 kb、1.07 kb、0.45 kb三个长度差异较大的目标位点。可见,试剂盒能在单个反应体系中兼顾各种长度的扩增子。
1:三重PCR;2-4:单重PCR;5-7:两重PCR。
M: DL5,000 DNA Marker



所有组分-20°C保存,有效期一年。
Q1:PM101一次可以扩多少个片段?酶的种类?扩增片段是否含有A尾,是否有5’-3’外切酶活性
A1:一次可以扩19个片段;为Taq酶;扩增产物末端有A;具有5’-3’外切酶活性。
Q2:跑PAGE胶,有很多弥散条带,有时候还有微笑条带
A2:建议延长延伸时间,降低循环数。
Q3:多重PCR跑胶后发现条带数量比目的条带数量少
A3:(1)条带全部扩增出来,因为条带设计的大小相近,跑胶未能区分开:建议将胶浓度提升、配置大长胶、延长跑胶时间;
(2)有些条带未成功扩增:前提需要重新跑胶进行鉴定,确定不是条带没有跑开:
①需要推荐引物设计原则:引物长度21 - 30 bp,GC含量40% - 60%,退火温度68°C以上;
②推荐目标片段不超过1500 bp;
③预先单独检测每对引物的扩增情况,尽可能挑选扩增特异性好的引物对进行组合;
④推荐每条引物反应终浓度为0.1 - 0.2 μM;
⑤如某些目标片段产量偏低,可适度提高其对应引物使用量以提高扩增产量;
⑥不同引物之间出现相互干扰:引物设计时,要避免不同引物之间出现序列互补的现象,以免互相干扰扩增。
Q4:多重PCR扩增产物少或没有扩增
A4:(1)模板
①使用高质量的模板,确认DNA模板纯度、浓度;
②增加模板使用量,25 μl反应体系中推荐模板量:人的基因组50 ng,质粒500 pg,cDNA 1 - 2.5 μl;
③扩增子GC含量过高或含有复杂二级结构时,推荐尝试Multiplex GC Enhancer;
(2)引物
①检查单对引物的扩增性能和特异性;
②使用高质量的引物,检查引物是否降解,确认每个反应中引物终浓度为0.1 - 0.2 μM;
③产物过长,重新设计引物;
④提高低产或缺失扩增子引物使用量。
(3)程序
①确认PCR程序预变性条件,以充分释放Multiplex DNA Polymerase活性。一般而言,抗体法热启动的酶预变性为30 s,进行直扩时可适当延长至5 min;化学法热启动的酶预变性为5-15 min;
②增加PCR循环数;
③降低退火温度(间隔1 - 3℃),必要时进行退火温度梯度尝试。确认退火时间为90 sec,必要时可延长退火时间至3 min;
④延长循环内延伸时间、延长彻底延伸时间。
Q5:多重PCR出现杂带,每对引物单独做PCR没有杂带
A5:主要是引物多了,错配的概率变高了。可以通过检测杂带的序列,判断是什么引物错配引起的。对于多重PCR来说,延伸时间非常重要,延长延伸时间有利于均一性。
Q6:存在非特异性扩增
A6:(1) 减少循环数;
(2) 提高退火温度;
(3) 减少引物使用量;
(4) 重新设计引物;
(5) 扩增子高GC或含有复杂二级结构时,推荐尝试Multiplex GC Enhancer,添加终浓度为0.5 - 1.0 ×。
Q7:电泳时条带模糊
A7:(1) 减少循环数(每次减少3个循环);
(2) 减少起始模板量;
(3) 延长彻底延伸步骤时间至15 - 30 min;
(4) 降低电泳电压,更换新的电泳缓冲液。
相关产品
GR501-01/02
G102-01
MD101-01/02
MD102-01/02
P071-01
P022-01/02





